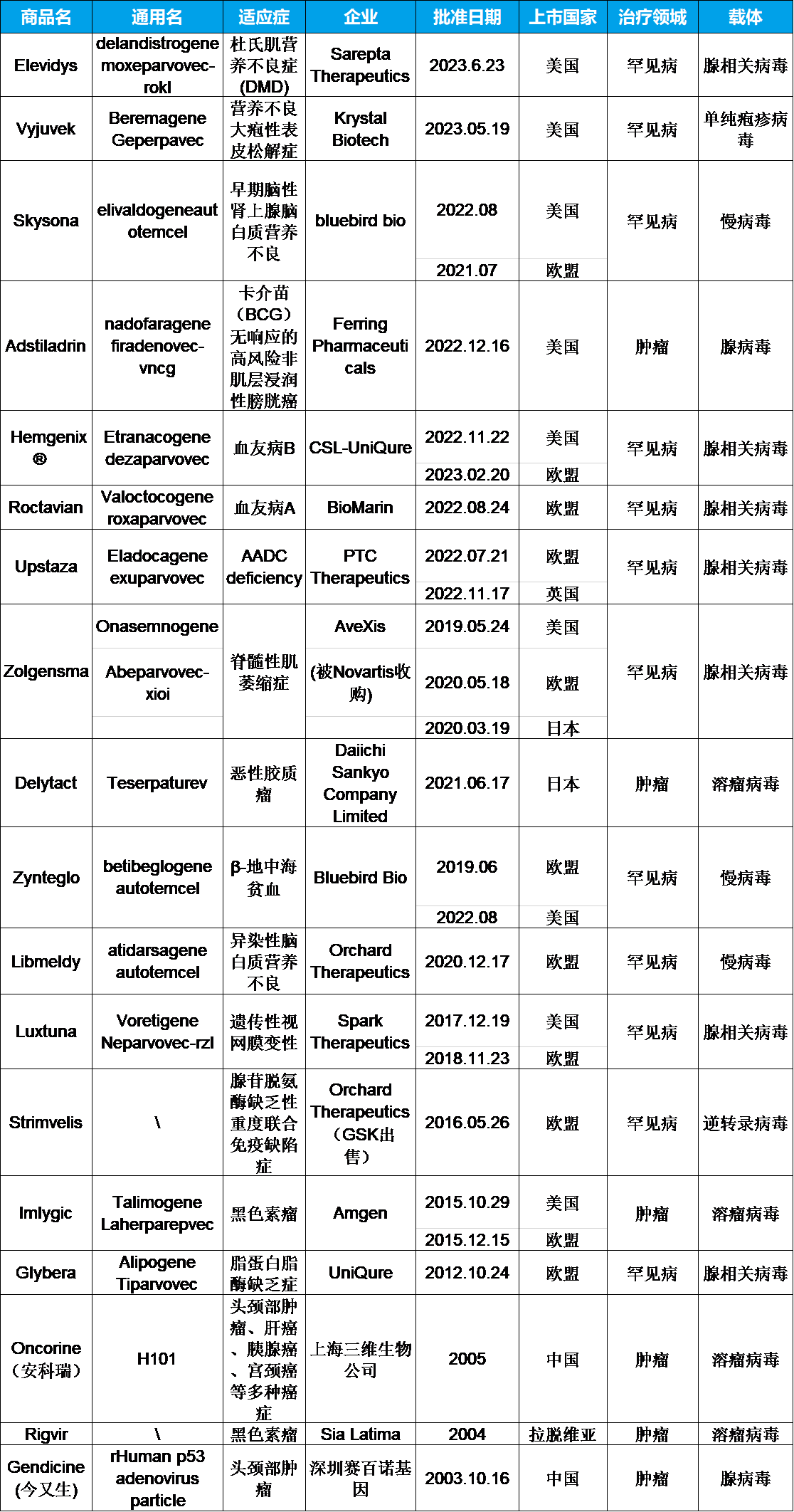Information
发布时间:2023-11-16

基因治疗是指将外源正常基因通过载体导入靶细胞,以纠正或补偿因基因缺陷和异常引起的疾病,以达到治疗基因缺陷疾病的目的。 截至目前,全球18款以病毒为载体的基因治疗药物获批(表1),递送载体层面,腺相关病毒(AAV)载体占主导。 表1 全球获批的18款以病毒为载体的基因治疗药物 (行诚生物整理) 随着递送系统不断成熟,基因治疗已逐步走向快速发展的黄金赛道,管线和企业层出不穷,研发热情空前。 AAV载体生产的挑战 机遇与挑战并存,进入到临床阶段或者是商业化阶段的AAV载体药物面临一个巨大挑战,即病毒载体大规模生产的产能短缺和成本高昂。对于眼科等局部病毒递送的适应症而言,对药物需求量不大,目前产能可以满足,但对于大量的需要全身递送载体的基因治疗适应症,如血友病,则对病毒载体的用量要求巨大,目前的产能远远达不到临床的要求。目前产能提升主要靠扩大生产规模来解决,但是产能建设耗资巨大且难度较高,从建设到投入使用往往需要近2年时间。另一方面,仅仅扩大规模,病毒包装生产批间稳定性的控制又是一个挑战,申报时生产方需要提供足够的CMC信息以确保基因治疗产品的安全、有效,质量可控。 AAV载体生产的主要技术体系有HEK293三质粒共转染系统和昆虫细胞杆状病毒包装系统(Bac/Sf9)。其中HEK293三质粒共转染系统由于其起步快、周期短、感染效率高、操作简便、安全性较高等优点,成为实验室及制药工业领域最常用的AAV生产方法之一。但由于其较为依赖GMP级质粒生产,贴壁培养的可放大性有限,产量较低,生产成本居高不下,甚至间接导致了“史上最贵疗法”的诞生。 可线性放大的AAV工艺 行诚生物技术团队迎难而上,对HEK293病毒包装工艺进行了大量研究和优化,最终开发出500L悬浮培养病毒包装工艺,不仅单位病毒滴度得到了大幅提高,而且该工艺可从PD小试规模直接线性放大至500L甚至2000L,目前500L规模已生产10+批次,工艺稳健性得到验证。293细胞上游表达量达到1E+12vg/ml,处于行业领先水平,下游工艺不用超速离心步骤,病毒满壳率依然可以达到>85%的水平,对于时间和成本的节省清晰可见。 无层析的质粒工艺 另外,病毒生产所需的质粒也是影响成本的一个重要方面。AAV在生产时多采用293细胞三质粒共转染法,拿100L病毒生产规模来算,一个批次质粒需求量约在1g左右,所以质粒成本的降低会间接降低AAV生产成本。 行诚生物在质粒工艺上同样进行了非常深入并且细致扎实的工艺开发和优化,并创新性地成功开发出了领先的质粒无层析的生产工艺。用基因稳定,超螺旋含量高,稳定性好的克隆制备菌种库,用优化的发酵条件和培养基提高了发酵阶段的质粒产量和质量,超螺旋纯度达90%以上。在下游纯化中优化了裂解澄清步骤,更加完全地从细菌中释放质粒,提高产率并非常有效地控制过程中产生的杂质,产品质量与3步层析工艺可比甚至更优,HCP、HCD、内毒素等的控制都保持在行业领先水平。无层析工艺可以极大地降低工艺过程所需缓冲液体积,商业化生产的成本将比业内平均水平降低60%。 以终为始的CMC考量 行诚生物拥有具有丰富商业化经验的CMC资深专家团队,以终为始在工艺优化中全面考量CMC,为客户完成了3个中美IND申报项目,服务的范围包括质粒,病毒和mRNA。行诚生物开发的工艺有严格的过程控制,得率高,可重复,可放大。切实帮客户升级产能、降低成本、少走弯路、少踩坑。 扫码了解更多详情或报价