Information
发布时间:2024-03-24

2024年1月19日,CDE发布了《重组腺相关病毒载体类体内基因治疗产品临床试验申请药学研究与评价技术指导原则》。作为CGT CDMO企业,行诚生物组织团队认真学习,今天小编就给大家分享一下其中质粒生产的要求。

《指导原则》在【生产用物料-起始原材料】的章节写明了质粒DNA需要提供的信息以及生产要求(如下截图),其中质粒生产应基于细菌种子批系统,采用适宜的方法纯化,并基于风险分析和产品特性对每批质粒进行质量检测,检测结果符合要求后方能用于载体生产。

从中大家不难发现,众所周知的层析工艺(包括三步、两步或一步)并非质粒纯化的唯一或必要方法,层析的核心目的是去除产品相关杂质(如开环、线性和多聚体质粒)以及工艺相关杂质(如宿主RNA、宿主DNA、宿主蛋白和内毒素等)。基于对质粒产品相关杂质的深入研究,通过工艺优化,产品相关杂质和工艺相关杂质可以在工艺流程得到有效控制和去除,就可以大大减少繁琐的质粒层析纯化步骤,甚至采用无层析工艺也可以很好地实现分离纯化的效果。无层析工艺纯化的质粒质量指标完全能够满足严格的质量放行标准,如AAV和LV病毒包装用质粒,mRNA模板用质粒和iPSC细胞基因编辑用质粒等。
行诚生物作为一家创新的CGT CDMO企业,始终行走在创新的前沿,致力于为行业提供更优质的工艺和服务。凭借对质粒DNA产品的深入理解和长期专注,公司对质粒工艺进行深度且细致扎实的工艺优化,并成功地实现了行业领先的无层析质粒工艺流程。
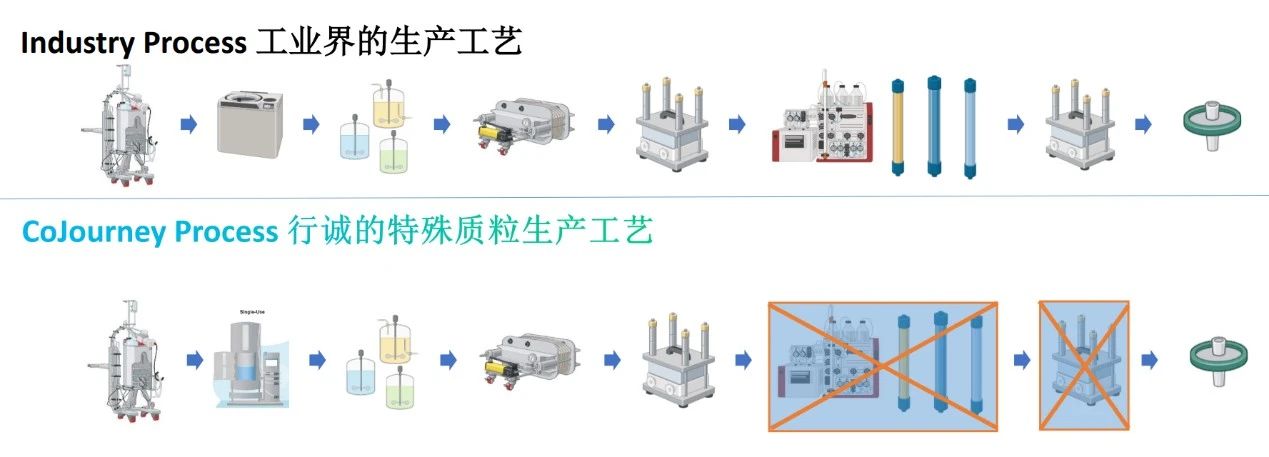
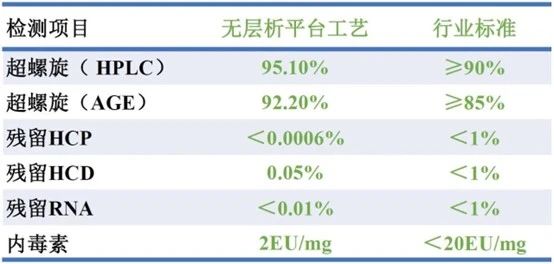
一些业内同行可能认为,实现无层析工艺是简单地用超滤技术替代了层析或采用其它有机溶剂沉淀方法,质疑这种纯化方式不可能达到与三步层析工艺同等的质量水平。然而,行诚生物的创新无层析质粒生产技术,正是基于公司丰富的CMC经验以及对工艺流程中产品和杂质的深入理解,并根据产品和杂质的不同生物学、物理学特性,精心设计工艺路线,控制过程参数,提高了产品的得率,减少了过程中对产品的破坏和杂质的产生,此外,通过对下游裂解工艺的优化,有效去除了大量杂质,实现了无需层析步骤就可以达到与传统的三步层析工艺可比甚至更优的产品质量,将与产品相关杂质和工艺相关杂质(HCP、HCD、HCR、和内毒素等)含量控制在行业领先水平。我们代表性的GMP批次终产品指标检测结果如下:
欢迎联系我们与技术团队沟通,并欢迎到行诚生物考察、交流、合作。

扫码留下您的联系方式,我们将安排技术人员与您沟通。

相关阅读
1.免层析质粒生产技术,通过工艺优化实现科学降本增效
2.个性化mRNA肿瘤疫苗迎来重大突破,如何解决“私人定制”的交叉污染挑战?
3.对质粒生产的交叉污染说NO!!!
行诚生物(CoJourney)是一家集质行诚生物(CoJourney)是一家集质粒、病毒载体、mRNA生产制备和分析检测为一体的专业基因和细胞治疗CDMO,有成功的中、美零发补质粒和病毒IND的申报经验。我们提供质粒、病毒载体和mRNA的制备工艺开发、cGMP生产、分析方法开发和产品检测放行等定制化服务。公司由基因和细胞治疗领域成绩斐然的科学家和具有商业化产业经验的资深专家共同创立,总部位于中国浙江和美国费城,业务辐射世界各地。同时,行诚生物建立了符合FDA、EU、NMPA法规的质粒和病毒cGMP生产设施,拥有世界领先的研发和生产仪器设备,提供从研发到cGMP级别的不同生产规模的质粒和病毒制备服务。我们用领先行业标准的稳健工艺确保为您提供高纯度、高产量、高性价比的优质产品和服务,赋能于您,成为您基因和细胞治疗产品开发旅程中值得信赖的合作伙伴!
CoJourney,践行“行之发于至诚”的理念,全心全意竭诚为您服务!