Information
发布时间:2024-04-17

随着技术的不断创新,产品的陆续上市,细胞和基因治疗(以下简称CGT)行业发展迅猛,前景无比广阔,引发生物医药行业人士越来越多的关注。在这个充满机遇与挑战的行业中,你关心哪些话题呢:
1.
IIT研究是每位从业者关心的焦点,它直接关系到治疗效果的评估与科学研究的进展。IIT研究有哪些挑战又如何保障受试者的安全和获益?医院筛选IIT项目的标准有哪些?IIT对于IND的影响是什么?
2.
同时,细胞基因治疗的高昂价格也是行业内外热议的话题,其背后的原因是什么?如何通过保险支付机制的设计推动治疗的可及性?
3.
此外,CMC在CGT产品的开发与生产过程中起着举足轻重的作用,和产品的安全性、有效性以及临床和上市申报密切相关。如何做好CMC是个大话题。
4.
而在这一充满变革与创新的领域遭遇经济寒冬之际,融资的重要性不言而喻,投资方如何看待这个市场又如何决策投资战略?
当然,还有很多技术创新的探讨话题:
5.
上游供应链尤其是国产供应链如何技术创新和降低成本满足行业需求,助力药品的可及?
6.
火热的AAV基因治疗的探索之路经历了什么,有哪些挑战,又如何展望?
7.
除了CAR-T,细胞治疗还有哪些火热的应用方向?溶瘤病毒、外泌体、干细胞、TIL?
8.
CGT在肿瘤和罕见病的探索进展如何?除此之外CGT还能在哪些领域大有作为,脱发、除皱了解一下?
你想知道的都在这里:Chat CGT。
Chat CGT是由E药经理人生命科学企业研究中心首席研究员、行诚生物商务副总裁刘肖博士发起和策划的栏目,每期邀请CGT研发和产业链企业领军者,从不同视角、多个维度分享CGT领域的挑战、解决方案、前沿进展和发展趋势。第一季12期已完美收官,小编特邀刘博士推出系列回顾文章,带你一起再次深入剖析和探讨这些关键话题,以期为行业的健康发展贡献一份力量。
第2期:
CGT商业化面临的困局

本期Chat CGT邀请到的嘉宾是复兴凯特高级商业准入总监汪祥宁先生和镁信健康首席创新官、高级副总裁冯昊先生。众所周知,2021年6月22日,复星凯特研发的CD19 CAR-T产品——阿基仑赛注射液(商品名:奕凯达®)正式在中国获批上市,成为中国首款以药品途径批准上市的CAR-T细胞治疗产品。本期内容围绕自体CAR-T产品的可及性展开讨论,以下是嘉宾关键观点梳理:

什么是CAR-T,治疗过程是怎样的?

人体的T细胞对感染、肿瘤、外来异物等有非常强的杀伤功能,也是构成我们免疫细胞的最重要的细胞之一。但是肿瘤细胞有肿瘤逃逸的功能,通过多种机制逃避机体免疫系统识别和攻击,也就是说T细胞找不到它。而CAR-T就是通过基因改造给T细胞装上了一个北斗导航(肿瘤嵌合抗原受体),能够特异性识别到肿瘤细胞进行杀伤从而达到治疗肿瘤的目的。
CAR-T的治疗机制是非常先进的,治疗方式也是特殊的,它是企业和医疗机构合作完成的一个治疗过程,全程需要30天左右,具体如下图:
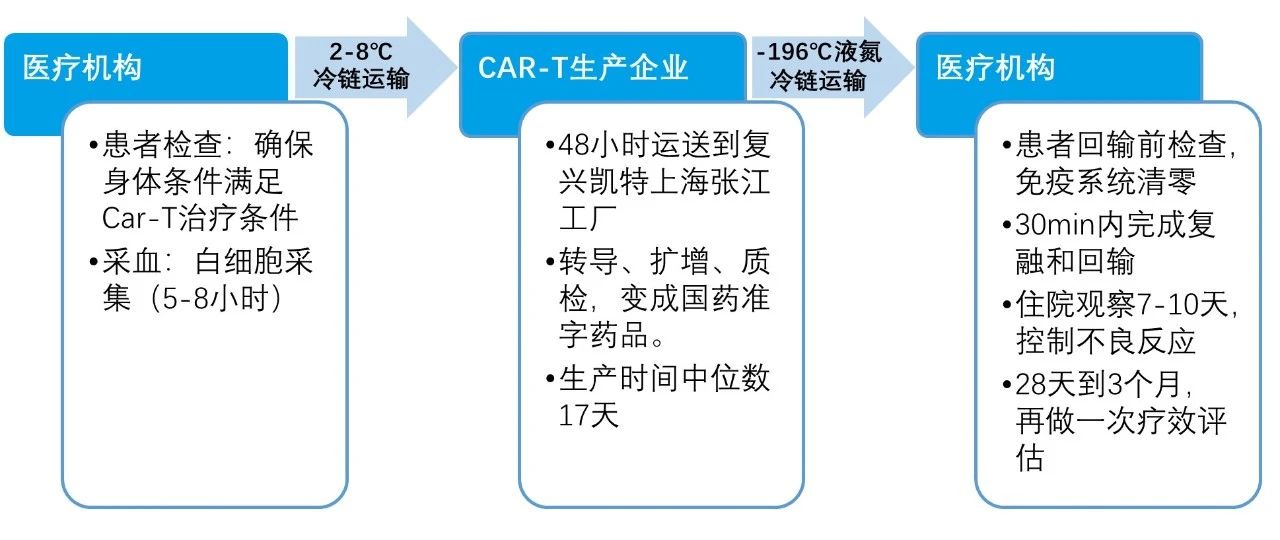

如何看待“120万一针治愈癌症”的媒体热议?

首先,这代表了人们对治愈癌症的热切期望和美好愿望。但目前CAR-T适应症主要集中在血液肿瘤,如奕凯达(阿基仑赛注射液)的适应症就是复发或难治性大B细胞淋巴瘤,当然,技术一直在进展中,国际上已经有骨髓瘤的CAR-T产品,对实体瘤的研究也在进行中,未来可期。但至少目前CAR-T并不能治愈所有癌症,所以一针治愈癌症一定要有个范围,不然就误导大家了。
其次,相比美国获批的同类产品30-40万美金的价格,120万人民币的价格已经是行业相对低的价格了。我们知道任何一个新技术面世之初通常都是高价的,如大家所熟知的计算机、移动电话等,因为它的突破性研究和面世所需要经历的严格的临床试验和审批程序等都是需要高昂的成本的。
最后,高昂的价格和CAR-T本身的生产制造过程和治疗过程相关。目前的CAR-T主要是自体化的产品,每一位患者就是一个批号,工厂为每一位患者定制生产,所以工业化生产的技术无法适用于自体CAR-T产品的生产制造,加之产品运送需要严苛的物流条件,这些是成本高昂的根本原因之一。

提高CAR-T的可及性,支付方和生产方都做了哪些努力?

商业保险为什么要纳入CAR-T?
宏观上,国家在2020年发布深化医疗保障制度改革,提到中国的医疗支付体系是以基本医疗保险为基础,各类商业医疗保险做补充,为人们提供更全面的保障。所以从顶层设计上商业保险有了更清楚的定位,商业保险公司有责任把人们真正有需求的好产品纳入保障体系。
微观上,五年前随着新特药的上市,患者的需求上升,大家意识到创新药处方药是需要被保障的,保险公司也积极推进,目前95%的新特药都纳入了保障。CAR-T同样作为一个创新的疗法填补了临床治疗的空缺,患者有需求,保险公司就有责任去纳入保障体系来。另外随着保险的保障体系搭建越来越好,能真正为患者提供全面保障,越来越多的人们认可商业保险,商业保险也会越来越积极的把更多真正需要被保障的产品纳入进来,这是一个良性循环。只有这样才能破解高价的CAR-T疗法甚至未来更高价的基因治疗的可及性难题。
支付方的角度,CAR-T是药还是手术,如何核算?
目前从国家监管的角度,明确是药品。商业保险的核算逻辑其实就是精算的逻辑,最关键的是要知道CAR-T疗法所对应的一系列的数据包括疾病的发病率、适用率等,以及在中国这个观念的教育程度等等,这样支付方才能更好的去判断这样的疗法被纳入商业保险时所对应的成本到底是多少。所以一个药品要纳入一款保险,这个过程需要和生产方、医疗机构等多方展开沟通合作,才能顺利完成。
生产方的战略:支付覆盖+压缩成本,两手抓
商业医疗保险对于提高药物可及性具有不可替代的作用。作为生产方,复兴凯特也把可及性作为一个最重要的战略去推动。2021年6月奕凯达上市之初,就积极推动纳入惠民保,7月份就被纳入了长沙惠民保,到目前为止奕凯达已经被94款惠民保纳入进去,也已经有很多的患者得到了实际的赔付。这有赖于和支付方、医疗机构积极主动的合作沟通,保持开放的心态,共同去完成保险精算模型,为保险设计和定价出力,确保未来的赔付能良性的发生,可控的发生,而不是等着保险公司自己去做。
另一方面,生产方积极优化生产流程,压缩生产成本。奕凯达整个的生产制造流程大概有600多个工序,对于工序的优化和主要原辅料的选择,复兴凯特技术团队都在积极的进行新的验证和探索,未来希望通过规模的提升,方法学的改进,为患者挤出更多的被惠及的空间。

安全性、有效性和可及性密不可分

安全性是药品的基础,有效性是药品存在的意义,二者缺一不可,且和可及性密不可分。安全性和有效性不够,可及性会受限。好的安全性和有效性会加速药品的可及。
CAR-T产品的生产是在严格的GMP工厂和质检规程中生产,质量是有保证的。备受考验的是治疗过程的两端是在医疗机构,在医疗机构中的采血过程以及中间的物流过程对于治疗的安全性是极其重要的。复兴凯特通过自己的探索,形成了一套非常完整可靠的方法学:和国内头部的血液病医疗机构合作,培训、认证并向国家备案近150家治疗中心,均达到奕凯达的使用能力以及不良反应的管理能力。
在这个过程中复兴凯特也成为了非常多标准的引领者,比如和上海医药行业协会以及上海药品评审中心建立了自体CAR-T供应链全国团体标准,和中国医药商业协会建立了自体CAR-T零售药房的服务规范。通过这些标准的建立为行业奠定很多规范化操作的基础,通过这些基础和方法学的累积,构建的质量保障的体系越来越完善,越来越可靠。值得一提的是复兴凯特目前所有交付都是百分之百合格的交付,在实践当中也证明了所构建的质量保障体系的可靠性。
截止目前,奕凯达已成功治疗逾600位淋巴瘤患者,基于良好的有效性数据,2023年6月21日,复星凯特提交的奕凯达®新适应症上市申请获得国家药监局正式批准。这也标志着,一线免疫化疗无效或在一线免疫化疗后12个月内复发的成人大B细胞淋巴瘤患者将加快获益,迎来治愈希望。
支付方为更好的满足人们治愈的需求,会找市场上疗效最好的产品纳入保障。未来实现按疗效支付也是有可能的,因为它是一种筛选更好疗效产品的方案。
结语
回首两年前,CAR-T产品初上市时面临的困难已经被大大的解决了,行业被理解,产品被认识,加之政策强有力的推动和支付方积极的参与,得以让这个先进的疗法两年来惠及了600位患者。我们相信未来会有更多的支付方参与进来,更好的方法、更好的模型,更多的患者被真正的惠及,获得治疗和治愈的希望。
商业保险为先进疗法的支付近几年呈现快速增长态势,随着人们对商业保险的认可和商业保险纳入更多先进疗法形成良性循环,相信未来商业保险会持续纳入更多更高价的先进疗法,即使已经有疾病的人们也能加入的保险未来也会问世,为患者提供更全面的保障,也让先进疗法可及性得到全方位的拓展。
看回顾不过瘾,扫码观看回放视频吧!

相关阅读:
行诚生物(CoJourney)是一家集质粒、病毒载体、mRNA生产制备和分析检测为一体的专业基因和细胞治疗CDMO。有成功的中、美零发补质粒和病毒IND的申报经验。我们提供质粒、病毒载体和mRNA的制备的工艺开发、cGMP生产、分析方法开发和产品检测放行等定制化服务。公司由细胞和基因治疗领域成绩斐然的科学家和具有商业化产业经验的资深专家共同创立,总部位于中国浙江和美国费城,业务辐射世界各地。同时,行诚生物建立了符合FDA、EU、NMPA法规的质粒和病毒cGMP生产设施,拥有世界领先的研发和生产仪器设备,提供从研发到cGMP级别的不同生产规模的质粒和病毒制备服务。我们用领先行业标准的稳健工艺确保为您提供高纯度、高产量、高性价比的优质产品,赋能于您,成为您基因治疗产品开发旅程中值得信赖的合作伙伴!
CoJourney,践行“行之发于至诚”的理念,全心全意竭诚为您服务!